Navigation auf uzh.ch
Navigation auf uzh.ch
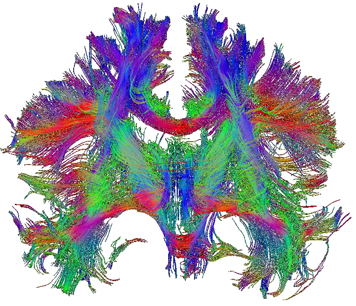
Die Diffusionstensor-Bildgebung misst die brownsche Bewegung (Diffusion) der Wassermoleküle im Gehirn. Die Diffusion der Wassermoleküle ist entlang von Nervenfasern stärker ausgeprägt als parallel zu den Fasern. Diese unterschiedliche Diffusionsstärke kann aus den Diffusionsdaten berechnet werden. Sogenannte Tracking Algorithmen erlauben anschliessend, die Nervenfasern im Gehirn aufgrund der Diffusionsrichtungen virtuell zu berechnen und zu rekonstruieren. Eines der grössten Probleme bei DTI basiertem Tracking ist, dass Kreuzungen und Verzweigungen von Fasern in einem Voxel nur sehr schwierig aufgelöst werden können. Q-Ball Imaging als neue Entwicklung in der Diffusionsbildgebung kann in Verzweigungs- und Kreuzungssituationen bessere Tracking-Resultate liefern.
Die Technik der Diffusionsbildgebung ist zurzeit die einzige Möglichkeit, die Struktur der Myelo-Architektur im menschlichen Gehirn in-vivo, nicht-invasiv und quantitativ zu erforschen. Sie erlaubt es, eine Approximation des strukturellen Netzwerks der Nervenfasern zu berechnen und darzustellen. In Verbindung mit funktionellen fMRI Daten kann erforscht werden, wie die funktionalen Areale im Cortex strukturell miteinander verbunden sind.
Under construction
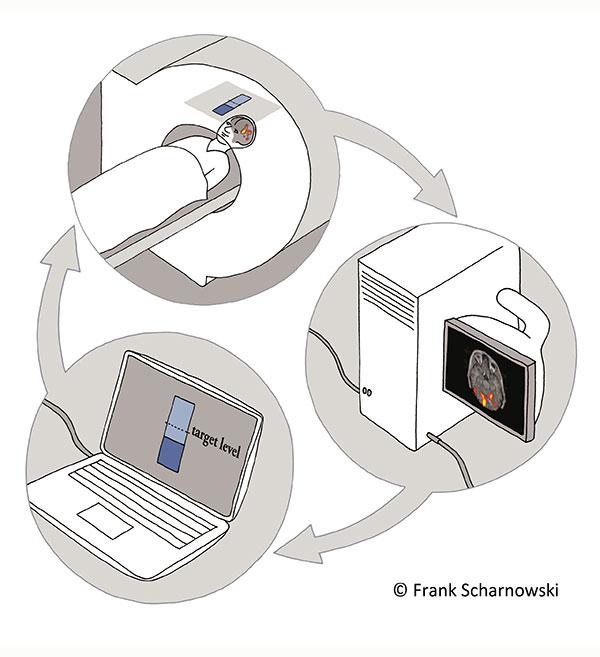
In der Psychiatrie wurde die funktionellen Magnetresonanztomographie (fMRT) bisher hauptsächlich zur Diagnose von abweichender Hirnaktivität bei psychiatrischen Störungen eingesetzt. Die Echtzeit-fMRT erlaubt nun den Einsatz der fMRT als therapeutisches Mittel. Indem wir die gemessene Hirnaktivität in Echtzeit analysieren und den Patienten darstellen, können diese lernen, ihre eigne Hirnaktivität zu kontrollieren. Ein solches Neurofeedback-Training ermöglicht es Patienten, die aufgrund ihrer Störung abweichende Hirnaktivität zu normalisieren. Neurofeedback ist eine nicht-invasive experimentelle Therapie, die auf die individuellen Bedürfnisse eines jeden Patienten angepasst werden kann, die biologische sowie psychologische Aspekte der Störung beachtet, und die auf einer wesentlichen menschlichen Eigenschaft gründet: Unserer Fähigkeit zu lernen.
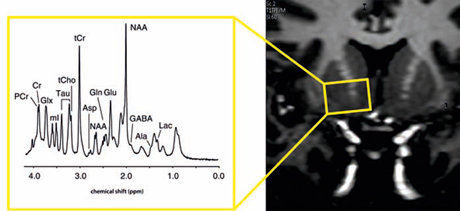
Die Magnetresonanz-Spektroskopie (MRS) ist eine nicht-invasive Methode, um die Konzentrationen von Metaboliten und Neurotransmittern im Körper zu bestimmen. Sie wird unterstützend zur klinischen Differenzialdiagnose eingesetzt (z.B. Tumoren, neurodegenerative Erkrankungen) und stellt darüber hinaus eine wichtige Methode zur Erforschung physiologischer und molekularer Biomechanismen dar. Die genaue Quantifizierung von Metaboliten und Neurotransmittern wie Glutamat (Glu), Glutamin (Gln) und Gamma-Amino-Buttersäure (GABA) ist neben Glukose (Glc) und N-Acetyl-Aspartat (NAA) von besonderem Interesse, da ein Grossteil der Informationsübertragung im Gehirn durch diese Metaboliten vermittelt wird. Sie spielen daher eine wichtige Rolle in der Pathophysiologie zahlreicher psychiatrischer Erkrankungen wie der Depression, Schizophrenie oder Angststörungen. In enger Zusammenarbeit mit dem Institut für Biomedizinische Technik (ETH & Universität Zürich) setzen wir neu entwickelte und für psychiatrische Fragestellungen optimierte MRS-Verfahren ein (z.B. 2D JPRESS). Diese kommen sowohl in Studien zu den neurobiologischen Grundlagen psychiatrischer Erkrankungen wie Depression oder Sucht als auch in klinischen Studien als prädiktive und therapeutische Biomarker zum Einsatz, um das Ansprechen auf verschiedene therapeutische Interventionen (z.B. Antidepressiva, Elektrokrampftherapie) zu erforschen.

Funktionelle Magnetresonanztomographie (fMRT) wird in der Psychiatrie benutzt, um Hirnaktivität bei Gesunden oder bei Menschen mit psychischen Erkrankungen zu messen. Was aber macht ein Hirnbereich genau, wenn er "aktiv" ist? Um diese Frage zu beantworten, benutzen wir mathematische (computationale) Methoden und Modelle. Diese erlauben (a) Rückschlüsse auf komplexe neuronale Prozesse, die nicht als globale "Aktivierung" eines grösseren Hirnbereichs aufscheinen (multivariate Auswerteverfahren wie MVPA und RSA), und (b) Rückschlüsse auf die genauen Berechnungen, die grosse Gruppen von Nervenzellen ausführen. Diese Methoden sollen uns verstehen helfen, warum einzelne Hirnbereiche bei bestimmten psychischen Erkrankungen mehr oder weniger "aktiv" sind als bei Gesunden. Wir arbeiten eng zusammen mit dem Wellcome Trust Centre for Neuroimaging und dem Max Planck UCL Centre for Computational Psychiatry and Aging, beide am University College London.